yl6809永利官网杨朝勇教授课题组与李清彪课题组及厦门大学附属中山医院王效民团队合作,提出了基于微流控芯片技术的肿瘤液体活检新方法,相关研究结果以“Isolation, Detection and Antigen Based Profiling of Circulating Tumor Cells Using a Size Dictated Immunocapture Chip”为题在《德国应用化学》上发表(Angew. Chem. Int. Ed. 2017, doi:10.1002/anie.201702675)。
循环肿瘤细胞(CTC)是从肿瘤组织脱落进入外周血的各类肿瘤细胞的总称,是导致肿瘤扩散的关键因素。与经典组织活检相比,基于CTC检测的液体活检技术具有肿瘤分子信息全、侵入性小、取样方便、成本低等优势,已成为目前最具发展潜力的肿瘤无创诊断和实时疗效监测手段之一,在肿瘤分期诊断、动态监测、用药指导和疗效评估等方面具有重大意义。CTC检测的最大困难在于其在外周血中含量稀少,而背景干扰却相当复杂。通常1 mL 外周血中含有109个红细胞,106个白细胞,而可能只含有1-10个CTC,在如此庞大复杂的正常细胞背景干扰下,很难实现高灵敏、高特异的CTC 捕获检测。
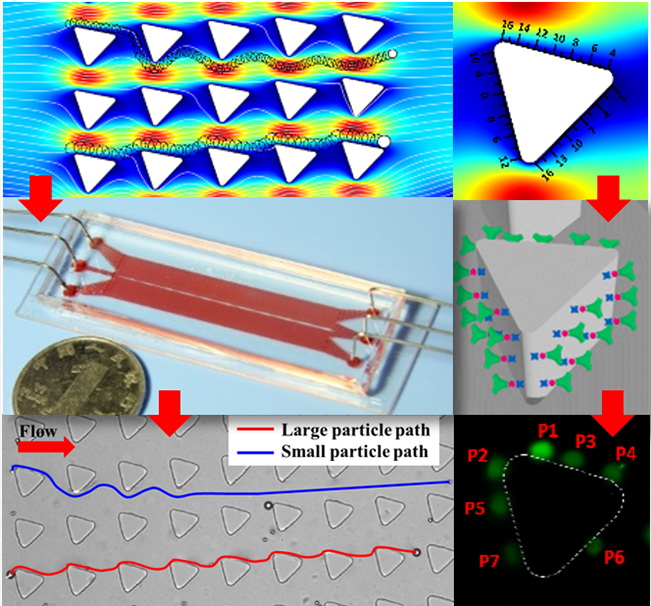
杨朝勇教授课题组针对这一挑战性课题,发展了基于流体力学分离与免疫识别的CTC捕获富集芯片(SDI-Chip)。该芯片内构建了成千上万个表面修饰有抗体的微柱阵列。微柱阵列排布方式根据确定性侧向位移分离原理设计,CTC因尺寸较大将沿微柱偏移方向运动并不断与微柱碰撞而实现特异性识别捕获,而血细胞因尺寸较小沿沿液流方向运动且很少与微柱碰撞而避免非特异性吸附。该设计有效地结合CTC在物理性质及表面标志物与背景细胞的差异,实现了CTC的高效、高纯度协同捕获。通过对大量临床肿瘤病人外周血样品的测试,该团队验证了所发展的芯片技术在肿瘤分期诊断、疗效监控等方面的潜在应用价值。
近年来,杨朝勇课题组瞄准精准医学对生物医学检测提出的新要求,发展了一系列检测新原理、新装置与新方法。该课题组发展了新型智能响应水凝胶材料传感技术,巧妙地利用血糖仪实现了复杂体系内非血糖目标分子的快速、便携、灵敏、定量检测 (J. Am. Chem. Soc. 2013, 135, 3748);提出了基于距离检测的新方法,利用类似温度计的读数方式实现了重要生物分子的可视化定量检测 (Angew. Chem. Int. Ed. 2014, 53, 12503);提出基于气压的生物检测新原理,发展了小分子、肿瘤蛋白等靶标的高灵敏定量便携检测新装置和新方法 (Angew Chem Int Ed 2015, 54, 10448); 发展了分子探针新方法与液滴微流控新技术,实现了单分子与单细胞的高通量操控与表征(J. Am. Chem. Soc., 2012, 134, 18908,Acc. Chem. Res., 2017, 50, 22)。
该工作第一作者Metages Gashaw Ahmed来自埃塞尔比亚,是化学工程与生物工程系博士研究生。该工作在国家杰出青年科学基金(批准号:21325522)、优秀青年基金(批准号:21422506)、基金委创新研究群体基金(批准号:21521004)等项目的支持下,历时三年,由厦门大学多个课题组协同攻关完成。
文章链接: http://onlinelibrary.wiley.com/doi/10.1002/anie.201702675/abstract
